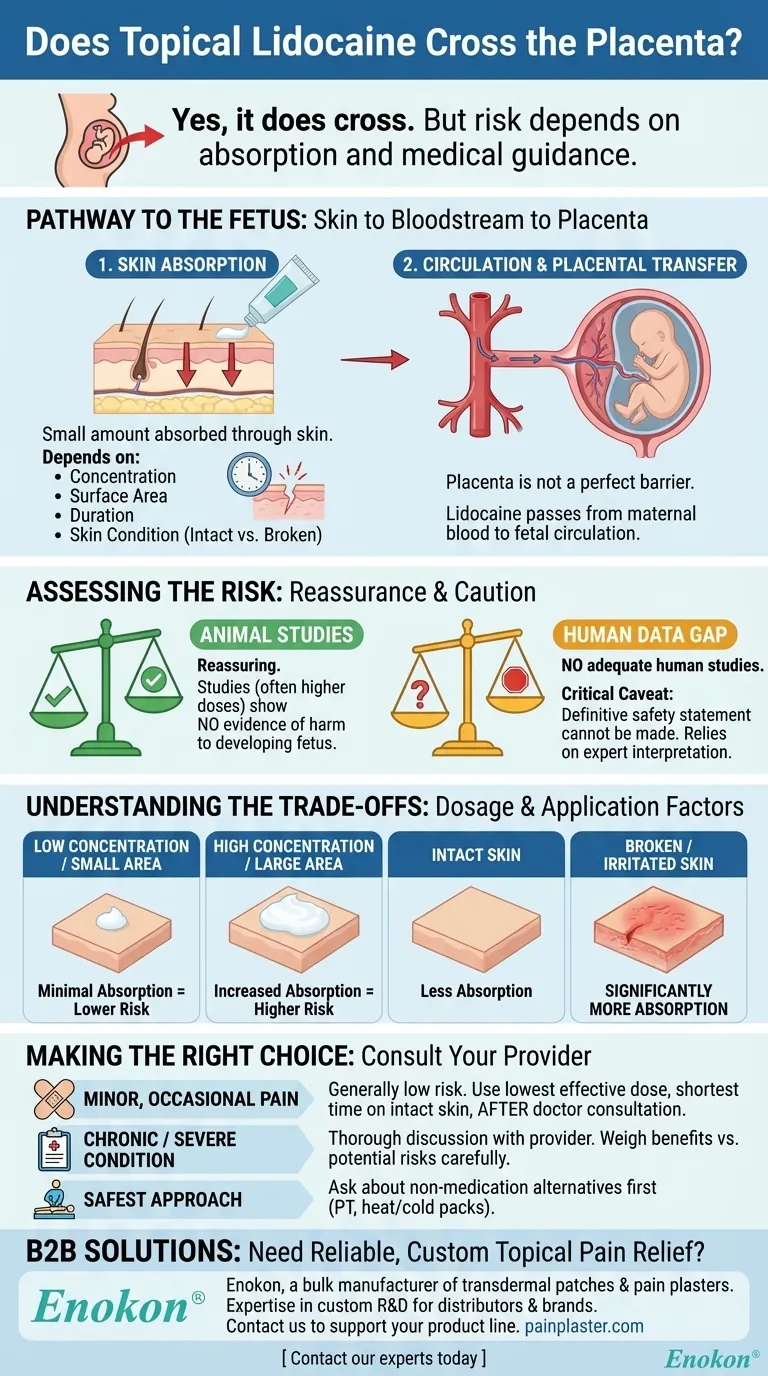
La lidocaïne topique traverse le placenta, mais les données disponibles issues d'études animales ne suggèrent aucun effet nocif significatif sur le fœtus.Cependant, il n'existe pas d'études humaines complètes permettant de confirmer pleinement sa sécurité pendant la grossesse.Il convient donc d'adopter une approche prudente dans l'utilisation clinique, en mettant en balance les avantages potentiels et les risques théoriques.

Explication des points clés :
-
Transfert placentaire de la lidocaïne topique
- La lidocaïne, lorsqu'elle est appliquée localement, peut traverser la barrière placentaire.Cela est dû à ses propriétés moléculaires, qui lui permettent de traverser les membranes biologiques, y compris le placenta.
- L'ampleur du transfert dépend de facteurs tels que la dose, le site d'application et le métabolisme maternel.
-
Études animales et sécurité fœtale
- La recherche animale n'a pas démontré de dommages directs pour les fœtus exposés à la lidocaïne.Ces études sont essentielles pour les évaluations initiales de la sécurité, mais ont des limites pour prédire les résultats chez l'homme.
- Les résultats suggèrent que les doses thérapeutiques typiques ne provoquent pas d'effets tératogènes ou d'anomalies du développement dans les modèles animaux.
-
Absence d'études humaines
- Il n'existe pas d'études bien contrôlées ou à grande échelle chez les femmes enceintes permettant d'établir avec certitude l'innocuité de la lidocaïne pendant la grossesse.
- Ce manque de données signifie que les prestataires de soins de santé s'appuient souvent sur des études animales et sur leur jugement clinique lorsqu'ils envisagent d'utiliser la lidocaïne.
-
Considérations cliniques
- La décision d'utiliser la lidocaïne topique pendant la grossesse doit tenir compte de la nécessité (par exemple, soulagement de la douleur lors d'interventions mineures) et des risques potentiels.
- Des traitements alternatifs ou des anesthésiques à moindre risque peuvent être envisagés s'ils sont disponibles.
-
Directives réglementaires et professionnelles
- Les organismes de réglementation classent la lidocaïne comme un médicament de "catégorie B" pour la grossesse, indiquant qu'il n'y a pas de risque prouvé chez les animaux mais que les données humaines sont insuffisantes.
- Les directives professionnelles recommandent souvent une utilisation minimale et une surveillance étroite si la lidocaïne est jugée nécessaire.
Bien que la lidocaïne topique soit généralement considérée comme présentant peu de risques, son utilisation pendant la grossesse doit être soigneusement évaluée au cas par cas.Avez-vous discuté de scénarios spécifiques dans lesquels la lidocaïne pourrait être essentielle pour le confort ou la sécurité de la mère ?
Tableau récapitulatif :
| Considérations clés | Détails |
|---|---|
| Transfert placentaire | La lidocaïne traverse le placenta en raison de ses propriétés moléculaires. |
| Résultats des études animales | Aucun effet nocif significatif n'a été observé chez les fœtus d'animaux aux doses thérapeutiques. |
| Lacunes dans les données humaines | Études limitées chez les femmes enceintes ; recours aux données animales et au jugement clinique. |
| Catégorie de grossesse (FDA) | Catégorie B : Pas de risque prouvé chez l'animal, mais études humaines insuffisantes. |
| Recommandation clinique | Utiliser avec prudence, en évaluant les bénéfices par rapport aux risques ; envisager des alternatives si possible. |
Besoin de solutions sûres pour soulager la douleur pendant la grossesse ?
À
Enokon
nous sommes spécialisés dans
les patchs transdermiques et les pansements anti-douleur conformes à la FDA
offrant
un soutien personnalisé en matière de R&D
pour les distributeurs et les marques de soins de santé.Nos formulations privilégient
la sécurité et l'efficacité
Même pour les populations sensibles comme les femmes enceintes.
Contactez nos experts dès aujourd'hui pour discuter des des options d'analgésie topique à faible risque adaptées à vos besoins.
Guide Visuel
Produits associés
- Patch antidouleur en hydrogel de lidocaïne pour le soulagement de la douleur
- Patchs anti-douleur à chaleur infrarouge lointaine Patchs transdermiques
- Patch cicatrisant en silicone Patch médicamenteux transdermique
- Patch anti-douleur Icy Hot Menthol Medicine
- Patch anti-douleur au gel de menthol
Les gens demandent aussi
- Un médecin généraliste continuera-t-il systématiquement à prescrire des patchs de lidocaïne après la période initiale ?Comprendre les directives d'utilisation à long terme
- Qu'est-ce qu'un patch de lidocaïne et comment fonctionne-t-il ?Explication du soulagement ciblé de la douleur
- Quels sont les effets secondaires courants des patchs à la lidocaïne ?Gérer les risques pour soulager la douleur en toute sécurité
- Quel est le patch le plus efficace contre l'arthrite ?Trouvez le meilleur soulagement pour vos douleurs articulaires
- En quoi les patchs de lidocaïne diffèrent-ils des patchs Icy Hot et Biofreeze dans leur mécanisme d'action ?










